WeissKruszka综合征和无法确定神经元身份
Weiss-Kruszka综合征是一种罕见的神经发育障碍,其特征是颅面畸形、发育迟缓和自闭症特征。奥地利科学院分子生物技术研究所(IMBA)和洛杉矶南加州大学(USC)凯克医学院的研究人员揭示了Weiss-Kruszka综合征的分子机制:基因的致病突变ZNF462导致在早期胚胎发育过程中无法保护神经谱系规范。该研究在疾病模型小鼠细胞中进行,于1月5日发表在《自然细胞生物学》上。
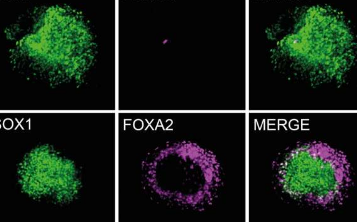
编码异染色质调节因子的基因突变通常与神经发育障碍(NDD)相关。异染色质,紧密堆积的DNA,被认为通过表观遗传染色质修饰强制谱系非特异性基因的转录沉默来稳定神经细胞的特性和功能。然而,大多数异染色质修饰符普遍表达并且缺乏序列特异性。因此,目前尚不清楚基因沉默的精确靶向是如何被控制的,以及异染色质修饰物的突变是如何导致NDD相关的神经元缺陷的。
IMBA和USC的研究人员现在发现了将异染色质调节剂G9A/GLP靶向染色质以在早期神经发生过程中抑制谱系非特异性基因的分子机制。他们发现以前未表征的小鼠锌指蛋白ZFP462直接与G9A/GLP相互作用。通过这样做,ZFP462在小鼠胚胎干细胞和神经祖细胞中的中胚层和内胚层特异性基因的增强子处建立了抑制性异染色质。未能将G9A/GLP靶向Zfp462突变细胞中的非神经元增强子导致它们的异常表达。这反过来又导致神经细胞对中胚层和内胚层细胞谱系的错误指定。
在人类中,直系同源ZNF462基因的一个等位基因突变会导致一种罕见的遗传疾病,称为Weiss-Kruszka综合征,并呈现自闭症谱系障碍的高置信度风险。根据小鼠细胞的结果,Weiss-Kruszka综合征患者的神经病理学可能是由神经细胞规格缺陷引起的。
ZFP462和早期胚胎中的细胞谱系规范
“我们证明ZFP462在保护早期小鼠胚胎细胞的神经谱系规范方面起着关键作用,”第一作者和共同通讯作者RameshYelagandula说,他在前IMBA小组组长OliverBell的研究小组做博士后期间开始了这个项目.在他们的研究中,Yelagandula、Bell和他们的团队表明,ZFP462介导的G9A/GLP募集促进了非神经增强子异染色质的形成。异染色质限制激活转录因子的结合,并阻止参与中胚层和内胚层细胞谱系规范的基因表达。因此,ZFP462对于促进外胚层特性至关重要,这样神经元细胞才能正常发育。
保护神经元细胞身份
“导致外胚层、中胚层和内胚层的三种细胞谱系在胚胎发育过程中很早就出现了,”最后一位和共同通讯作者贝尔说。外胚层细胞进一步分化为神经元细胞和组织,如神经、脑和脊髓。“一旦确定了不同的细胞谱系,保持它们的特性对于保护特定细胞和组织的功能至关重要,”Yelagandula说。细胞身份的丧失会导致发育缺陷并导致疾病。因此,需要通过异染色质调节剂进行有效的表观遗传沉默,以维持谱系规范和细胞身份。
可能的未来疗法?
ZNF462是与Weiss-Kruszka综合征有关的基因,在脊椎动物中高度保守。通过表征小鼠直系同源物Zfp462的机制,新发现揭示了一种罕见的人类神经发育障碍的可能分子机制。“我们的数据表明,Weiss-Kruszka综合征可能是由早期胚胎发生过程中神经元谱系中谱系非特异性基因的异常激活引起的,”Bell说。
研究人员正在考虑可能的应用来帮助治疗受影响的患者。诊断为Weiss-Kruszka综合征的患者仅携带ZNF462的一个突变等位基因,其中包含一个提前终止密码子,而第二个等位基因是有功能的。由于仅存在一个正常等位基因,因此功能蛋白的水平降低。
“我们目前正在研究突变等位基因是否会产生一种截短的、可能错误折叠的蛋白质,这种蛋白质在ZFP462调节中具有显性负性作用。如果是这种情况,我们可能能够通过中和截短的蛋白质进行干预,并帮助减轻患者的症状,”叶拉甘都拉报告说。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。