研究人员发现有助于皮肤癌扩散到全身的蛋白质
由伦敦玛丽女王大学、伦敦国王学院和弗朗西斯·克里克研究所领导的研究发现了一种蛋白质,它使黑色素瘤(最严重的皮肤癌)更具侵袭性,它使癌细胞能够改变其细胞核的形状——一种允许细胞迁移和扩散到全身的特性。
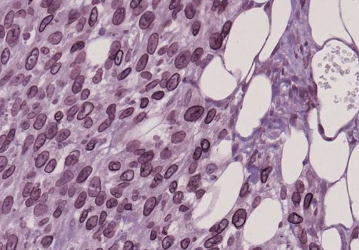
今天发表在《自然细胞生物学》上的这项研究模拟了侵袭性黑色素瘤细胞的行为,这些细胞能够改变细胞核的形状,以克服癌细胞在组织迁移时遇到的物理限制。该研究发现,这些侵袭性黑色素瘤细胞含有高水平的一种叫做LAP1的蛋白质,这种蛋白质水平的升高与黑色素瘤患者的预后不良有关。
黑色素瘤是一种可以扩散到身体其他器官的皮肤癌。癌症扩散或转移是癌症相关死亡的主要原因。虽然转移已被广泛研究,但其发生的机制却知之甚少。该研究的结果揭示了黑色素瘤进展的机制,并可能为开发针对黑色素瘤扩散的新方法铺平道路。
该研究由玛丽皇后学院巴茨癌症研究所的VictoriaSanz-Moreno教授以及伦敦国王学院和弗朗西斯克里克研究所的JeremyCarlton博士共同领导。
在这项研究中,该团队在实验室实验中挑战了侵袭性和侵袭性较低的黑色素瘤细胞,使其通过小于细胞核大小的人造膜中的孔迁移。侵袭性细胞来自黑色素瘤患者的转移部位,而侵袭性较低的细胞来自同一患者的原始或“原发性”黑色素瘤肿瘤。
为了转移,癌细胞需要脱离原发肿瘤,转移到身体的另一部分并开始在那里生长。然而,肿瘤致密的周围环境使癌细胞难以做到这一点。
细胞包含一个大而坚硬的结构,称为细胞核,它存储细胞的遗传信息,但也限制了细胞穿过肿瘤环境中的紧密间隙的能力。为了让癌细胞挤过这些缝隙,它们需要使细胞核更具延展性。
迁移实验后进行的成像显示,侵略性细胞能够通过在其细胞核边缘形成称为“泡”的凸起,比侵略性较小的细胞更有效地穿过孔隙。黑色素瘤细胞的遗传分析表明,形成泡的侵袭性细胞含有更高水平的LAP1蛋白,该蛋白位于细胞核周围的膜(称为核包膜)内。
杰里米·卡尔顿(JeremyCarlton)博士的实验室对了解细胞内膜结合结构的动力学很感兴趣,他说:“核膜被束缚在下面的细胞核上,我们的研究表明,LAP1蛋白松开了这种束缚,允许核膜膨胀并形成气泡,使细胞核更具流动性。结果,癌细胞可以挤过通常会阻止它们的缝隙。”
当研究小组在实验室实验中阻止侵袭性细胞中LAP1蛋白的产生并再次挑战它们通过孔迁移时,他们发现细胞形成核包膜泡的能力较差,也不太能够挤过这些缝隙。
该团队还在来自患者的黑色素瘤样本中观察到相同的LAP1表达模式。与原发性肿瘤中发现的水平相比,从黑色素瘤患者转移部位采集的组织样本中的LAP1水平更高。原发肿瘤边缘细胞中LAP1水平高的患者癌症侵袭性更强,预后更差,这表明该蛋白可用于识别可能具有更高侵袭性疾病风险的黑色素瘤患者亚群。
Sanz-Moreno教授的研究小组有兴趣了解癌细胞如何与环境交流以促进其生长和扩散,他说:“黑色素瘤是最具侵袭性和致命性的皮肤癌。通过结合我实验室的专业知识Carlton博士的研究,我们对LAP1如何促进黑色素瘤的进展获得了新的机制理解,并表明LAP1是实验室和患者模型中黑色素瘤侵袭性的关键调节因子。”
“因为LAP1在转移细胞中的表达水平如此之高,干扰这种分子机制可能会对癌症扩散产生重大影响。目前还没有直接靶向LAP1的药物,因此展望未来,我们希望研究靶向的方法LAP1和核膜起泡,看看是否有可能阻止这种黑色素瘤进展的机制。”
该团队想研究由LAP1驱动的核包膜起泡是否发生在构成和穿过肿瘤环境的其他细胞(例如免疫细胞)中,以确定其他细胞中的这一过程是否有助于或阻碍癌症的进展。
英国癌症研究中心研究与创新执行主任IainFoulkes博士说:“像这样的研究是一个完美的例子......研究除了研究癌症对我们身体生物学的影响外,还加深了我们对癌症的了解。专注于诊所中发生的事情。
“这种对黑色素瘤细胞核如何变得更加流动以在身体周围移动的新认识有助于建立我们对癌症如何运作的知识,并开辟了一条新的研究途径,以研究使癌症更难扩散的方法。“
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。