用于多模态成像和协同光疗的聚集金纳米颗粒偶联物
新加坡国立大学的化学家发现,聚集的光敏金纳米颗粒偶联物可用于多模态成像和协同光疗,以低于皮肤耐受阈值的功率密度有效破坏癌细胞。该研究发表在《今日纳米》杂志上。
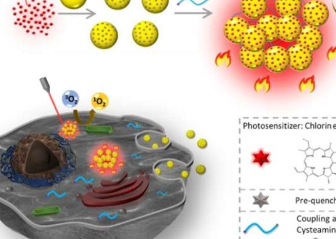
光疗技术,如光动力疗法(PDT)和光热疗法(PTT)因其微创性而引起了广泛的兴趣,成为治疗癌症的有前途的治疗技术。在PDT中,光敏剂被激活以产生活性氧,从而在光照射下破坏癌细胞。
对于PTT,光热剂用于吸收光辐射能量并将其转化为热量以破坏癌细胞。然而,传统的PDT存在“始终开启”模式,具有严重的治疗后副作用和活性氧的低效生成。PTT处理还具有一些缺点,例如过热造成的不必要损坏以及将光热剂输送到目标部位的效率相对较低。
新加坡国立大学化学系徐庆华教授领导的研究团队设计了一种基于共轭金属纳米颗粒的光敏剂聚集诱导发射增强方案。这些纳米颗粒具有多模态成像能力,并以其聚集形式具有高效的PDT/PTT协同治疗效果。
在该方法中,Chlorine6共轭金纳米颗粒的聚集体显示出显着增强的一光子和双光子激发荧光,单线态氧生成和光热效应。光敏剂的光活性首先通过将它们附着在金纳米颗粒上来抑制,但当它们形成聚集体时,光活性显着增强。除了增加亮度外,纳米颗粒聚集体的光稳定性与其非聚集形式相比显着提高。这是由于激发态分子的寿命缩短。
根据他们的发现,研究人员已经展示了在实验室条件下使用HeLa癌细胞的多模态成像和协同光疗。通过在癌细胞内原位形成聚集体,纳米颗粒聚集体分别在红光和近红外光的单光子和双光子激发下充当荧光成像探针。这些纳米颗粒聚集体还表现出优异的PDT和PTT性能,由于协同治疗效果,使用功率密度低于皮肤耐受阈值的红光激光器可以有效地破坏癌细胞。
徐教授说:“这种基于新型聚集诱导发射现象的等离子体纳米系统为成像引导PDT/PTT协同治疗提供了一种有前途的技术。这可能会为探索安全、准确和无创的治疗诊断学开辟一个新的场所。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。