新研究显示突触可塑性在调节癫痫患者脑功能中的关键作用
癫痫是一种以大脑过度电活动为特征的神经系统疾病,其发病机制尚不清楚。现在,使用一种新型放射性示踪剂([11C]K-2,第一种可视化和量化活人脑中α-amino-3-hydroxy-5-methyl-4-isoxazolepropionicacidreceptor(AMPAR)的技术),来自日本的研究人员已经能够深入了解AMPAR运输在癫痫发生中的作用。他们的发现可能会导致针对癫痫患者的新型疗法的开发。
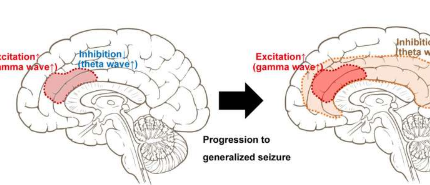
癫痫——一种导致反复无端癫痫发作的神经系统疾病——影响着全世界数百万人。虽然大脑电节律的不平衡被认为是导致癫痫的主要因素,但其潜在的病理生理机制仍然难以捉摸。
现在,在CellReportsMedicine上发表的一项研究中,由横滨市立大学的研究人员领导的团队已经能够研究癫痫患者的大脑功能,并阐明这种疾病的生物学基础。
使用正电子发射断层扫描(PET)和脑电图(EEG),该团队分析了α-amino-3-hydroxy-5-methyl-4-isoxazolepropionicacidreceptors(AMPARs)在癫痫发生中的作用。“AMPAR在大脑的突触可塑性中起着关键作用。因此,我们最近开发了一种PET放射性示踪剂,[11C]K-2,这是第一个也是唯一一个可用于量化AMPAR密度的技术。活人脑。这种示踪剂使我们能够研究AMPAR密度与脑电图测量的大脑动态电活动之间的关系,”横滨市立大学医学研究生院的TakuyaTakahashi教授解释说,他是该研究的主要作者.
神经元突触促进信息在神经元之间的传递。然而,突触功能障碍会导致各种脑部疾病,包括癫痫。突触可塑性——神经元活动引起神经元之间连接强度变化的过程——主要以两种形式存在:赫布可塑性和稳态可塑性。赫布可塑性促进了信息在神经元中编码和保留的机制,而稳态可塑性使神经元回到其原始状态。目前的研究基于这样一个前提,即涉及AMPAR的突触可塑性故障会触发癫痫发生。
为了深入了解癫痫发生的生物学机制,研究人员监测了癫痫患者体内放射性标记的AMPAR的运输情况。他们发现细胞表面AMPAR密度与局灶性癫痫的伽马活动振幅呈正相关。此外,从局灶性发作到全身性发作的转变伴随着正AMPAR-theta活动耦合的消失和负AMPAR-theta活动耦合的扩散。这一结果具有极其重要的意义,因为据报道,局灶性至双侧强直阵挛性发作是癫痫猝死的最重要危险因素。
研究人员还发现,在局灶性癫痫发作的患者中,AMPAR运输的增加也增加了异常伽马活动的幅度,这从EEG测量中可以明显看出。相反,全身性癫痫发作的患者细胞表面的AMPAR减少。这种减少与异常伽马活动幅度的增加有关。研究人员还指出,癫痫患者的AMPAR水平低于健康对照组。与局灶性癫痫发作的患者相比,全身性癫痫发作的患者在更大的皮质区域中也表现出较低的AMPAR水平。
“鉴于这些发现,我们认为赫布可塑性增加AMPAR运输和稳态缩放以补偿癫痫发作中突触功能的下调可以调节癫痫脑功能,”高桥教授说。
总而言之,该团队的发现平息了对人类癫痫生物学基础的若干疑问,并可能导致针对患有这种疾病的患者开发出新颖有效的疗法。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。