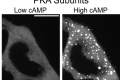
迷你结肠模仿结直肠癌发展中的健康肿瘤组织
洛桑联邦理工学院(EPFL)的科学家和其他机构的同事利用微加工、组织工程和光遗传学技术,成功开发出能够在体外产生与体内肿瘤非常相似的肿瘤的微型结肠。他们的工作发表在《自然》杂志上,题为“体外迷你结肠中的时空解析结直肠癌发生”。
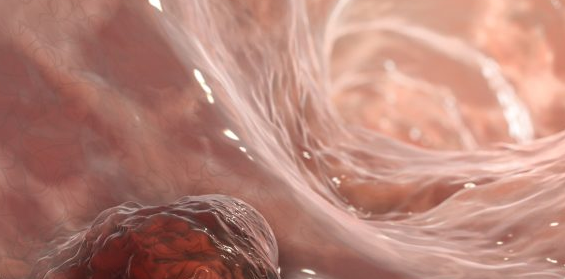
迷你结肠复制了结肠组织的物理结构,包括隐窝和腔结构,以及健康和患病状态下实际结肠组织中存在的细胞多样性。在肿瘤动力学中复制的能力使它们能够很好地减少药物发现和开发对动物模型的依赖。
研究人员表示,在复制实际结直肠肿瘤中看到的细胞行为和复杂组织结构方面,它们甚至可能比一些三维培养模型更好。作者在《自然》杂志上写道:“即使是目前基于类器官的黄金标准3D模型(通常被认为是体外和体内之间的桥梁),对于离体癌症发展建模也过于简化。”
此外,它们的寿命短、缺乏“拓扑生物学稳定性和一致性”以及“无法以平衡和整合的方式生成由健康细胞和癌细胞组成的混合组织”,使得它们不太适合作为研究肿瘤发展和药物反应研究的模型。
迷你结肠和使用相同方法开发的任何其他器官可能就是答案。研究小组表示,他们生成的组织可以“以稳定且与解剖学相关的拓扑结构复制干分化细胞模式轴;[可以]以时空受控的方式轻松突变和追踪;并创建一个生物力学动态系统,允许肿瘤出现,同时保持周围健康组织的完整性。”
也许迷你结肠最重要的特征是可以利用光诱导它们在目标区域形成肿瘤。光遗传学是一个利用光精确控制基因表达等生物过程的领域,科学家们利用光遗传学技术,将蓝光响应系统集成到迷你结肠中,看看它们是否能够有针对性地引导肿瘤发生。
正如预期的那样,当研究人员打开灯时,他们在结肠的特定细胞群中引入了致癌突变,模仿体内结直肠癌的局部发病。观察几周内肿瘤的出现可以揭示有关肿瘤行为和动态的大量信息。该研究的资深作者、洛桑联邦理工学院生物工程研究所教授MatthiasLütolf博士说:“这基本上可以让你实时观察肿瘤的形成,并对在小鼠身上很难研究的过程进行非常详细的分析。”。
一旦肿瘤形成,就可以对其进行研究。为了证明这一点,研究人员对结肠进行了筛选,寻找参与肿瘤发展的已知分子的证据。对结肠样本进行单细胞RNA测序揭示了GPX2蛋白的过度表达,该蛋白与干细胞特征和肿瘤生长相关。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。