研究人员揭示DNA修复机制
一项新的研究为细菌细胞如何持续修复其 DNA 缺陷部分的全新画面增添了新的色彩。
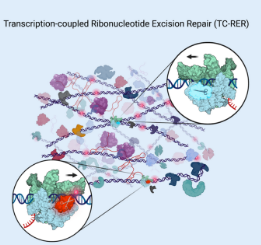
该报告于 5 月 16 日在线发表在《细胞》杂志上,描述了 DNA 修复途径背后的分子机制,该途径可防止错误地将某种类型的分子结构单元核糖核苷酸包含到遗传密码中。这种错误在细菌和其他生物体的代码复制过程中很常见。鉴于核糖核苷酸错误掺入会导致有害的 DNA 代码更改(突变)和 DNA 断裂,所有生物体都已进化为具有称为核糖核苷酸切除修复 (RER) 的 DNA 修复途径,可以快速修复此类错误。
去年,由纽约大学朗格健康学院生物化学和分子药理学系朱莉·威尔逊·安德森教授Evgeny Nudler博士领导的团队发表了两项对大肠杆菌活细胞 DNA 修复的分析。他们发现,某些类型的 DNA 损伤(大块损伤)的大部分修复,例如由紫外线照射引起的损伤,都是因为受损的代码部分首先被称为 RNA 聚合酶的蛋白质机器识别出来的。RNA 聚合酶沿着 DNA 链向下运动,读取 DNA“字母”的代码,同时将指令转录为 RNA 分子,然后指导蛋白质构建。
Nudler 及其同事发现,在这个转录过程中,RNA 聚合酶还会发现 DNA 损伤,然后作为组装称为核苷酸切除修复 (NER) 复合物的 DNA 修复机器的平台。然后,NER 剪掉发现的有缺陷的 DNA,并用准确的副本替换它。如果没有 RNA 聚合酶的作用,活细菌中几乎不会出现 NER(如果有的话)。
现在, Cell的新研究提供了第一个证据,表明与 NER 通路一样,RER 与转录紧密耦合。研究作者发现证据表明,参与 RER 的关键酶 RNaseHII 也与 RNA 聚合酶合作,因为它扫描活细菌细胞 DNA 链中错误掺入的核糖核苷酸。
“我们的研究结果继续激发人们重新思考 DNA 修复领域的某些基本原理,”Nudler 说,他也是霍华德休斯医学研究所的研究员。“展望未来,我们的团队计划研究 RNA 聚合酶是否扫描 DNA 以发现各种问题并触发全基因组修复,不仅在细菌中,而且在人类细胞中也是如此。”
尖端技术
核糖核苷酸(RNA 的组成部分)和脱氧核糖核苷酸(DNA 成分)是相关化合物。研究作者说,当细胞在细菌细胞中复制和构建 DNA 链时,它们经常错误地将核糖核苷酸代替脱氧核糖核苷酸并入 DNA 链,因为它们仅相差一个氧原子。在细菌细胞中,已知 DNA 聚合酶 III 每次复制细胞的遗传物质时都会犯大约 2,000 个这样的错误。为了保持基因组的完整性,大量错位的核糖核苷酸被 RER 途径移除,但一个关键问题是 RNaseHII 如何在完整细胞 DNA 代码的“海洋”中如此迅速地发现相对罕见的核糖核苷酸损伤。
正如他们在 2022 年的研究中所做的那样,研究人员使用定量质谱法和体内蛋白质-蛋白质交联来绘制化学连接蛋白质之间的距离,从而确定 RNaseHII 和 RNA 聚合酶在活细菌细胞中相互作用时的关键表面。通过这种方式,他们确定大多数 RNaseHII 分子与 RNA 聚合酶偶联。
此外,他们使用低温电子显微镜 (CryoEM) 捕获与 RNA 聚合酶结合的 RNaseHII 的高分辨率结构,以揭示定义 RER 复合物的蛋白质-蛋白质相互作用。此外,削弱 RNA 聚合酶/RNaseHII 相互作用的结构导向遗传实验损害了 RER。
“这项工作支持一种模型,在该模型中,RNaseHII 在 RNA 聚合酶沿着 DNA 移动时扫描 DNA 以寻找错位的核糖核苷酸,”第一研究作者、Nudler 实验室的博士后学者 Zhitai Hao 说。“这项工作对于我们对 DNA 修复过程的基本理解至关重要,并且具有深远的临床意义。”
除了 Nudler 和 Hao,纽约大学医学院生物化学和分子药理学系的研究作者还有 Manjunath Gowder、Binod Bharati、Vitaly Epshtein、Vladimir Svetlov 和 Ilya Shamovsky。该研究得到了国立卫生研究院、霍华德休斯医学研究所和布拉瓦尼克家庭基金会的支持。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。