前列腺细胞的二维遗传图谱描绘了癌症的生长
我在8月10日发表在《自然》杂志上的一项研究中,科学家们以高分辨率绘制了人类前列腺的遗传图谱,并发现额外或缺失的染色体块(称为拷贝数变异)如何被认为是癌症所特有的,通常存在于看似健康的组织中.
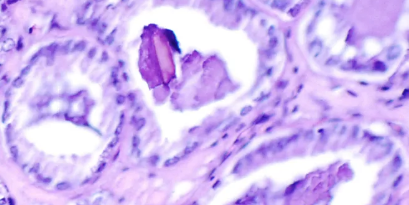
“这出人意料且完全出乎意料,”该研究的合著者、牛津大学纳菲尔德外科科学系的泌尿科医生AlastairLamb说。“我们认为这些变化定义了前列腺癌。但它们存在于完全良性的[组织]中。”
肿瘤远非均匀的细胞团,而是由恶性、良性和健康组织拼凑而成。了解正常细胞如何癌变需要科学家绘制出这个复杂生态系统中的遗传变化。Lamb的团队与瑞典KTH皇家理工学院的基因技术研究员JoakimLundeberg及其同事合作,使用一种称为空间转录组学的技术将拷贝数变异映射到前列腺内的精确位置。
与大量DNA测序等方法不同,在这些方法中,细胞被撕裂,有关其物理位置的任何信息都丢失了,空间转录组学通过在测序前用位置数据对RNA分子进行基因标记来保留样本的3D结构,从而使每个序列都可以匹配到其在器官内的原始位置。
空间转录组学协议的图形描述
通过前列腺切除术从癌症患者身上切除的整个前列腺被水平切成组织切片,然后进一步分成块。使用空间条形码探针捕获单个块的mRNA并测序。这使研究人员能够查看在DNA(inferCNV)或基因表达谱(转录组学)中推断的拷贝数变异是否映射到显微镜下确定为癌变的区域(共识病理学)。
这涉及将组织切片放在包含点网格的玻璃表面上,每个点都锚定包含空间条形码和一串与mRNA分子结合的胸腺嘧啶残基的短核苷酸链。组织样本在被放置在玻璃上之前会被透化,这样mRNA就会溢出细胞,使其附着在网格上,从而标记每个分子在组织内的位置。
在这项研究中,研究人员想要创建一张老年患者手术切除的前列腺内拷贝数变化图,因此他们使用包含30,000个点的网格拖网组织横截面以获取转录本。每个点对应于只有十个细胞的区域,捕获了从离它最近的细胞释放的大约3,500个mRNA分子,使团队能够绘制基因表达图。然后,使用计算方法,该团队使用他们测序的RNA来预测细胞DNA中的拷贝数变异,并确定基因相同的细胞簇或克隆。然后,他们将这些克隆组装成系统发育层次结构,以绘制细胞的遗传组成如何随时间发生变化的图表。
与此同时,该团队在显微镜下观察了完整的组织,以根据形态学对癌变和良性组织区域进行注释。Lamb说,将成像数据与空间遗传图谱相结合揭示了单个肿瘤内的惊人数量的异质性,低级别肿瘤细胞(那些更接近健康细胞的细胞)位于健康和进一步进展的高级肿瘤之间细胞。正如预期的那样,癌细胞包含MYC和肿瘤抑制基因PTEN等致癌基因的拷贝数变异。然而,令人惊讶的是,附近的健康组织也发生了同样的变化。
“这里最棒的是二维快照。我们看到了非常早期的事件、中间事件以及肿瘤已经分化,”Lundeberg说。他将这项技术与组织学取样进行了对比,在组织学取样中,病理学家在显微镜下识别肿瘤并使用激光对其进行解剖。Lundeberg说,这可以提供对肿瘤的详细了解,但忽略了它周围的细胞环境。“但是通过空间转录组学,您可以捕获在显微镜下观察时不明显的早期事件。”
约翰霍普金斯大学的癌症研究员ElanaFertig对这种癌症遗传学的全器官方法感到特别兴奋,她没有参与这项研究。“我认为这是不可思议的,这是我们越来越需要做的事情。我们要确保我们不会遗漏可能不在主要病变中的复发分子标记,”她说。
为了研究类似的模式是否出现在其他类型的癌症中,Lundeberg及其同事使用皮肤癌、乳腺癌和胶质母细胞瘤的组织切片重复了该过程。和以前一样,他们在肿瘤细胞和附近的健康组织中发现了染色体改变。
这些发现表明拷贝数变异发生在良性细胞转化为恶性组织之前,而不是之后,伦敦国王学院的癌症遗传学家FrancescaCiccarelli说,他没有参与这项研究。“看似正常的细胞具有与肿瘤相关的[拷贝数变异]的观察结果表明它们不足以进行转化,”她在给TheScientist的电子邮件中写道。
这就提出了一个问题,即如果不是这些拷贝数变异,是什么遗传事件驱动了肿瘤发生。Lamb表示,该研究中未调查的DNA变化,例如表观遗传修饰,可能发挥重要作用。“在癌症克隆和周围的基质组织之间也存在[化学]信号传导的可能性,”他补充道。
然而,捕获显微镜下不可见的早期遗传事件可以让研究人员预测良性组织区域是否会导致致命癌症,这对早期诊断和靶向治疗具有重要意义。“那是如此,如此强大,”伦德伯格说。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。