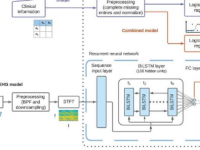
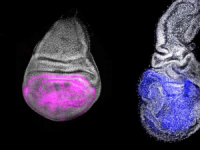
阻塞性睡眠呼吸暂停会破坏小鼠全天的基因活动
美国辛辛那提儿童医院医学中心的大卫史密斯及其同事在开放获取期刊PLOSBiology上发表的一项新研究表明,阻塞性睡眠呼吸暂停(OSA)的低血氧水平导致全天基因活动发生广泛变化。这一发现可能会导致早期诊断和追踪疾病的工具。
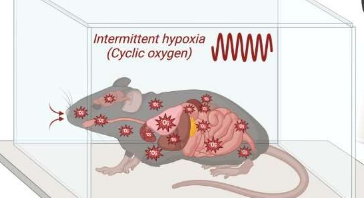
当气道被阻塞(通常被软组织阻塞,与夜间打鼾和呼吸中断有关)时,就会发生OSA,导致间歇性缺氧(低血氧)和睡眠中断。它影响着全世界超过10亿人,仅在美国每年的直接医疗费用就高达1500亿美元。OSA会增加心血管、呼吸系统、代谢和神经系统并发症的风险。
许多基因的活动在一天中自然变化,部分是响应生物钟基因的活动,其规律性振荡驱动多达一半基因组的昼夜节律变化。基因活性也会因外部因素而变化,包括氧气水平的降低,这会导致产生“缺氧诱导因子”,从而影响许多基因的活性,包括时钟基因。
为了更好地了解OSA如何影响全天的基因活动,作者将小鼠暴露在间歇性缺氧条件下,并全天检测六种组织(肺、肝、肾、肌肉、心脏和小脑)的全基因组转录。然后,作者评估了这些相同组织中基因表达的昼夜节律时间的变化。
最大的变化发生在肺部,间歇性缺氧影响了近16%的所有基因的转录,其中大部分基因被上调。只有不到5%的基因在心脏、肝脏和小脑中受到影响。
通常表现出昼夜节律的基因子集受到间歇性缺氧的影响更为强烈,肺中74%的此类基因和心脏中66.9%的此类基因发生了显着变化。在每个组织中受影响的基因中有已知的时钟基因,这种效应可能导致这些组织中其他基因的昼夜节律活动发生巨大变化。
史密斯说:“我们的研究结果为长期暴露于间歇性缺氧的患者终末器官损伤相关的病理生理机制提供了新的见解,并且可能有助于确定未来评估诊断或治疗方法的机制研究的目标;“例如,通过血液测试跟踪一种失调的基因产物来检测早期OSA。
BalaSCKoritala补充说:“我们使用阻塞性睡眠呼吸暂停动物模型的研究揭示了整个基因组转录组和相关标志性通路的时间和组织特异性变异。这些独特的发现揭示了与这种疾病相关的早期生物学变化,发生在多个器官系统。”
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。