研究人员确定了预防免疫疗法副作用的潜在新策略
加州大学洛杉矶分校琼森综合癌症中心的研究人员领导的一项研究表明,IL-21是一种参与激活免疫系统的可溶性分子,它可能是一个潜在的治疗靶点,有助于减少检查点抑制剂癌症治疗引起的内分泌自身免疫副作用。
研究人员发现,一组具有强大杀伤活性的特定CD8+免疫细胞,称为CXCR6+IFN-γ细胞毒性CD8+T细胞,在这种自身免疫攻击中起着核心作用。他们还发现了这些CD8+的活性受IL-21控制,阻断IL-21可防止甲状腺自身免疫。
“我们的研究首次深入研究了人类检查点抑制剂相关甲状腺自身免疫的原因,并强调了预防这种与治疗相关的自身免疫毒性的潜在途径,”医学助理教授MelissaLechner博士说。在加州大学洛杉矶分校大卫格芬医学院内分泌学、糖尿病和新陈代谢系工作,也是该研究的第一作者。
检查点抑制剂是一种癌症疗法,它利用免疫系统的力量来对抗癌细胞,并已证明在治疗多种类型的晚期癌症方面取得了显著成功。虽然这种类型的疗法改变了癌症治疗的面貌,但随着免疫激活的增加,可能会对健康组织造成不必要的自身免疫攻击。这种与免疫相关的不良事件发生在高达60%的接受治疗的患者中,并可能导致治疗中断、住院,甚至过早死亡。
这些自身免疫毒性的原因在很大程度上仍然未知。目前还没有有效的治疗方法来预防或逆转癌症免疫治疗过程中的这些内分泌免疫不良反应,这些不良反应几乎普遍导致永久性器官损伤和终生需要激素替代治疗。
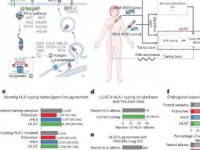
为了调查检查点抑制剂癌症治疗期间发生的自身免疫毒性的原因,研究小组对患者的甲状腺样本进行了单细胞RNA测序。该团队随后表明,表达CXCR6+颗粒酶B和干扰素-γ的克隆扩增效应CD8+T细胞在患有甲状腺不良事件的个体中增加。此外,他们发现来自CD4+T辅助细胞的IL-21驱动这些CD8+T细胞的甲状腺毒性功能,并且在小鼠模型中抑制IL-21可防止检查点抑制剂相关的甲状腺自身免疫。
研究结果突出了潜在的免疫通路,这些通路可以靶向降低患者的免疫治疗毒性。了解接受癌症免疫疗法治疗的患者自身免疫毒性是如何产生的,将有助于研究人员制定减少这些副作用的策略,使治疗更加安全。
此外,驱动癌症免疫治疗相关自身免疫的机制可能与自发性自身免疫性疾病相同,例如1型糖尿病和桥本氏甲状腺炎。因此,这项研究的发现还可以帮助研究人员确定治疗多种自身免疫性疾病的靶标。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。